今回は「異種金属接触腐食とイオン化傾向」についての記事です。
私は以前「異種金属を組合わせると腐食する」と聞いたことがあったのですが、それがなぜなのか?疑問に感じていました。
例えば、「鉄+ステンレス」や「鉄+アルミニウム」などです。基本的には同種の金属を組合わせると思いますが、このような組み合わせもありがちではないでしょうか?
そこで今回は、異種金属で腐食が起きるメカニズムについてまとめておこうと思います。
異種金属接触腐食とは
異種金属接触腐食(ガルバニック腐食)とは、電気が流れる水溶液中で電位の異なる金属を接触させると電池が形成されるため、電位の低い金属が溶け出し腐食し、電子のやり取りが起きることです。
*電気が流れる水溶液とは、電解液のことで電解質と呼ばれる水に溶けると陽イオンと陰イオンにイオン化(電離)する物質が溶けている水溶液です。電解質には塩化ナトリウム(食塩水)、塩化水素(塩酸)、塩化銅(塩化銅水溶液)、硫酸、水酸化ナトリウムなどが挙げられます。逆に、電気が流れない物質は非電解質と言います。
電位の異なる金属の特徴
-
電位が低い金属・・・卑金属と言う。イオン化傾向が高く腐食しやすい。アノード(電子を放出する側、負極側)となる。
-
電位が高い金属・・・貴金属と言う。イオン化傾向が低く腐食しにくい。カソード(電子が入ってくる側、正極側)となる。
*イオン化傾向については、次項で解説します。
腐食のイメージ図
*クリック拡大
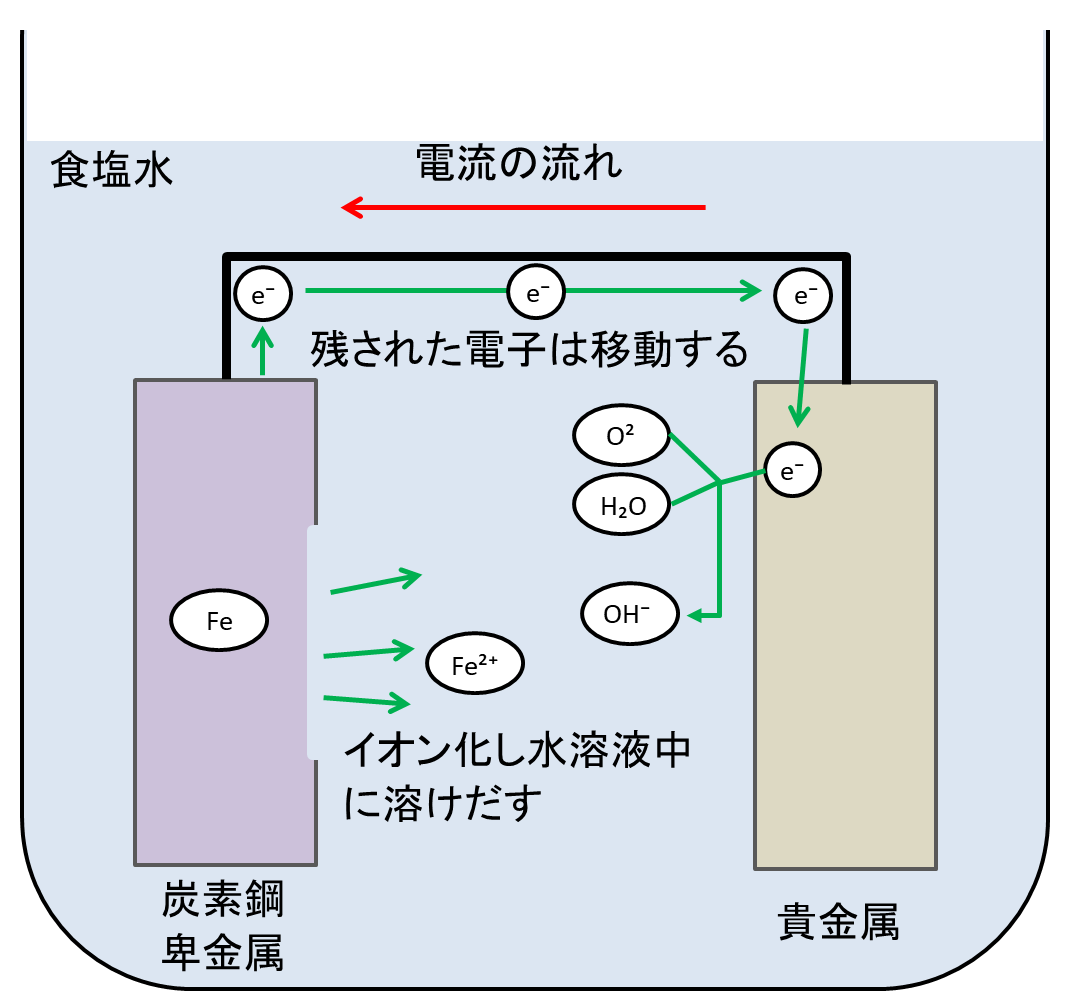
水溶液中で電位の異なる金属はどうなるのか?
-
電位の低い金属(卑金属)・・・「水溶液中に溶けだす(酸化)」=「原子が電子を放出して陽イオンになる」
-
電位の高い金属(貴金属)・・・卑金属に残った電子が、電位の高い金属に移動する(電流は逆に流れる)。電位の高い金属は電子を受け取り還元します。
*補足 電子と電流の流れる向き
電子と電流の流れる向きには注意が必要で、電流の流れは電子の移動とは逆向きとなります。
-
電子・・・負極(マイナス)から正極(プラス)へ移動する。
-
電流・・・正極(プラス)から負極(マイナス)流れる。
電子と電流の流れる向きが違い理由について、下記を引用します。
引用:北海道電気保安協会 電流のおはなし
電流の流れの方向は電子の流れと反対方向をいいます。
これは電気の研究を始めた昔、まだ電子が発見されていないときに正電気の流れる方向を電流の方向と定めたからです。
今考えると逆のわけですが、これは別に不都合がないので、現在も電子の流れとは逆の方向を電流の方向としております。
イオン化傾向と金属の腐食
異種金属接触腐食の説明で、イオン化傾向について触れましたので、ここからはイオン化傾向についてまとめておきます。
イオン化傾向とは、水溶液中で金属が電子を放出してイオンへの「なりやすさ」のことで、イオン化傾向が大きいほど「腐食(錆)」やすく、またイオンへのなりやすさは元素によって違いがあります。
イオンへのなりやすさは、イオン化列で表すことができイオン化列は標準電極電位の順番となります。
*標準電極電位とは?下記を引用します。
標準電極電位とは
ある単体を、そのイオンが1mol/L存在する溶液につけた場合において単体と溶液の間に生じる起電力(電位差)のことです。水素が基準となります。
それでは、イオン化傾向の一覧をご覧ください。
イオン化列
*クリック拡大
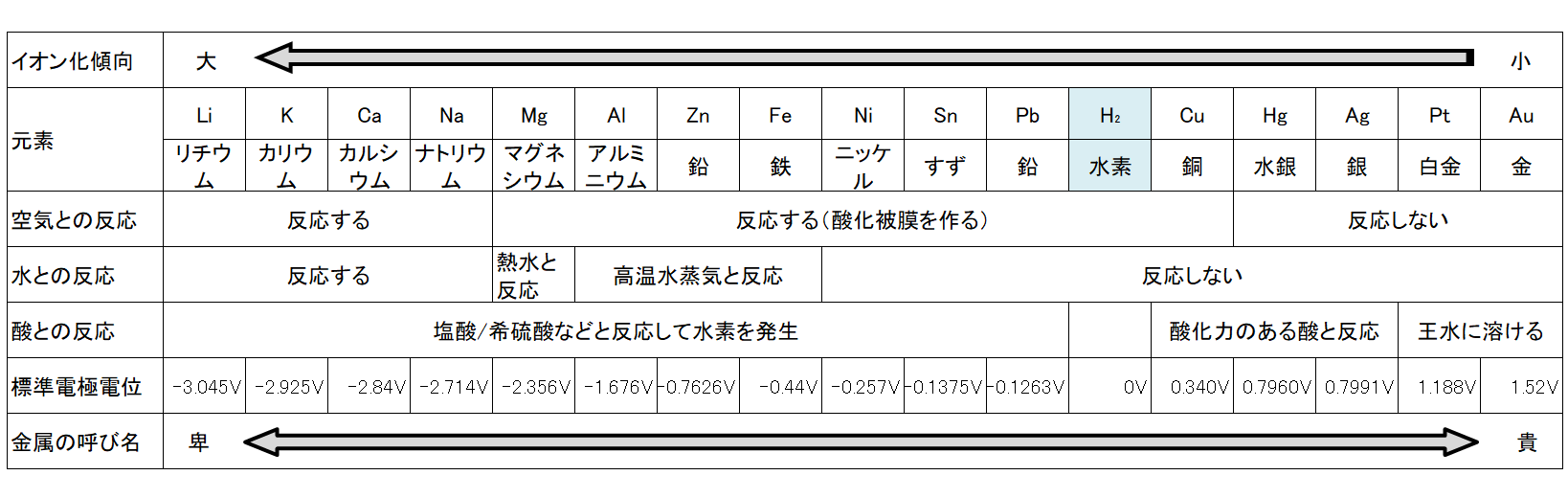
*補足 電位差による金属の呼び名
-
卑金属・・・電位が低い金属。イオン化傾向が高く腐食しやすい。アノード(電子を放出する側)となる。
-
貴金属・・・電位が高い金属。イオン化傾向が低く腐食しにくい。カソード(電子が入ってくる側)となる。
イオン化列をまとめますと、、
「電位が低い金属(卑金属)」=「イオン化傾向が高い金属」は水溶液中で酸化しイオン化するので腐食し易い
「電位の高い金属(貴金属)」=「イオン化傾向が低い金属」は水溶液中で電子を受け取り還元するので腐食しない
この様に解釈できると思います。
イオン化傾向の注意点
イオン化列で、金属の違いによる腐食のし易さが分かったと思いますが、ここで注意点があります。
それは、金属の電位は環境(金属が曝される状況)の影響で変化するので、イオン化列では予測がつかないことがあると言われています。
ですから、イオン化列だけで腐食のしやすさを判断しても、現実には当てはまらないことがあるようです。
また、異種金属の組み合わせで電位差があっても、電解質の水溶液(電流が流れる)が金属に接する状況でなければ腐食が起きないも考えられます。
もし、水溶液に接する場合でも、異種金属同士の接合に絶縁性の材料を組合わせて異種金属同士が絶縁できれば腐食を防ぐことができるのではないでしょうか。
補足 鉄とステンレスの腐食
私が実際に経験した異種金属の腐食の例を紹介します。
下記の写真をご覧ください。
これは「塗装の鉄」と「ステンレス」を組合わせた部品で、水が入った水槽に浸かっていた状態です。
鉄とステンレスの接触している部分で腐食が起きていることが確認できます。
鉄とステンレスの腐食
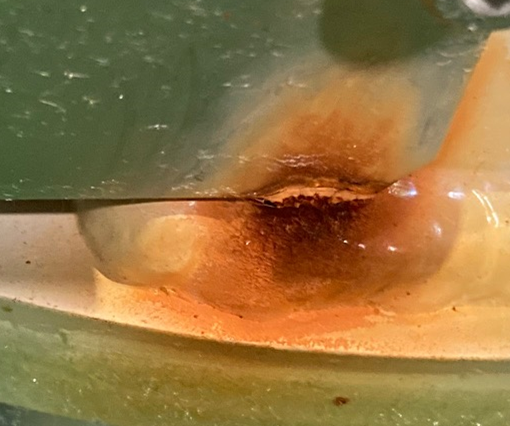
水道水の水に浸かっていたので、電気が流れる状態であったようです。
まとめ
今回は、異種金属接触についてまとめてみました。機械装置において、鉄、ステンレス、アルミの組み合わせで組立ることはよくあることだと思います。ですが、必ずしも腐食するとは限らず、電流が流れる状況が関係することでしょう。湿度が高かったり、水を使う場合、または鋼管(配管)を使用を必要とする機械装置は十分に配慮したいところです。
*腐食の勉強におすすめ
関連記事:【材料/溶接/加工/表面処理】
以上です。
